高齢期に必要な生活習慣病管理
公開日:2018年4月20日 17時34分
更新日:2024年8月14日 12時54分
こちらの記事は下記より転載しました。
荒木 厚(あらき あつし)
東京都健康長寿医療センター内科総括部長
生活習慣病とは
生活習慣病とは、食事、運動、睡眠、喫煙、飲酒などの生活習慣がその成因に深く関与していると考えられる疾患の総称である。糖尿病、高血圧、脂質異常症、肥満などの動脈硬化性疾患の危険因子となるものや、脳卒中、虚血性心疾患などが代表的な生活習慣病である。慢性腎臓病、肝硬変、慢性閉塞性肺疾患、がんも生活習慣病である。最近では認知症やフレイルも生活習慣病ではないかと考えられてきている。
この生活習慣病は、中年期と高齢期では違った考え方で治療することが必要である。例えば、中年期の肥満は認知症発症の危険因子となるが、高齢期の肥満は認知症発症のリスクにはならない1)。また、どの程度まで生活習慣病の治療を行うべきかという問題も、中年期と高齢期では異なる。日本老年医学会では、高齢者の糖尿病、高血圧、脂質異常症のガイドラインを作成し、肥満のガイドラインも作成中である。
本稿では上記4つの高齢者の生活習慣病の疾患を中心に、その意義や治療について解説したい。
心血管疾患発症の危険因子
高齢者の生活習慣病の心血管疾患発症の危険因子としての意義は、疾患や年齢で異なる。
中年期や前期高齢期の糖尿病における高血糖は合併症や死亡と関連するが、後期高齢者ではその関連が弱くなる。スウェーデンの追跡調査では、75歳未満の糖尿病患者ではHbA1cが増加するにつれて心血管死亡のリスクが増加したが、75歳以上ではHbA1c値の増加に伴う心血管死亡リスクの増加が軽度となり、HbA1c7.9%以上で初めて有意となった2)。一方、重症低血糖は高齢者の中でも加齢とともに起こりやすく、80歳以上で最も多くなる3)。
脂質異常症では主に前期高齢者で高LDLコレステロール血症が冠動脈疾患の危険因子である。一方、75歳以上の高齢者を対象とした研究では、LDLコレステロール値と冠動脈疾患リスクの間に関連性を認めないとする報告が多い4)。わが国のメタ解析では89歳の男性では総コレステロール240mg/dL以上で冠動脈疾患死が有意に増加したが、女性では関連が認められなかった5)。
一方、高血圧では80歳以上の高齢者を対象とした試験でも利尿薬ベースの降圧治療により脳卒中、心不全発症、全死亡、および心血管病による死亡が抑制されている6)。SPRINT研究の75歳以上でのサブ解析においても、通常治療よりも厳格な降圧が心血管イベントや死亡リスクを低下させている7)。高齢者高血圧では年齢にかかわらず生活習慣改善で降圧が不十分であれば積極的に降圧薬治療を行うべきである。
認知症発症の危険因子
高齢期の生活習慣病の中で糖尿病とメタボリックシンドロームは認知症発症の危険因子となる。糖尿病は中年期のみならず、80歳以上の高齢者糖尿病でも認知症発症の危険因子となる8)。高齢者のメタボリックシンドロームは認知機能低下や認知症発症と関連するという報告が多く、特に慢性炎症の存在下でその関連は強くなる9)。メタボリックシンドロームの構成要素の数が増えると認知機能低下を来たしやすい。しかしながら、75歳以上の高齢者においてはメタボリックシンドロームと認知機能低下との関連は明らかではない。
上記のように中年期の肥満は認知症発症の危険因子となるが、高齢期の肥満はリスクとはならず、やせや体重減少を来たした群で認知症になりやすい。
高血圧は高齢者における高血圧と認知症発症との関連については一定した報告がない。久山町研究では高齢期の血圧レベルがⅠ度高血圧での血管性認知症リスクは4.5倍であったが、アルツハイマー病との関連はみられなかった10)。また、血圧と認知症発症との関連はないという報告もある11)。
高齢期における血清LDLコレステロール値やトリグリセリド値と認知症発症に関しても一定の傾向を認めない。
ADL低下やフレイルの危険因子としての生活習慣病
高齢者の生活習慣病はADL低下の危険因子となるものが多い。メタ解析では糖尿病は手段的ADL低下が1.82倍、基本的ADL低下が1.65倍起こりやすい12)。高血圧も手段的ADL低下または基本的ADL低下の危険因子となる13)。
高齢期の肥満のみならず、中年期からの肥満ならびに身体活動性の低下は、高齢期のADL低下のリスクとなる14)。サルコペニア肥満は単なる肥満と比べて、よりADL低下・転倒・骨折、死亡を来たしやすい15)。
高齢者のメタボリックシンドロームがADL低下のリスクになるかについての報告は一致していない。高TG血症、低HDLコレステロール血症を含めた脂質異常症もADL低下と関連することを示す十分なエビデンスはない。ただし、アポE4はADL低下と関連する16)。
高齢者の生活習慣病の治療目的
高齢者の生活習慣病は、認知機能障害、ADL低下などの老年症候群を来たしやすい。老年症候群とは高齢者に多い医療、看護、介護を要する症状や徴候の総称である。特に糖尿病では、認知症、ADL低下、サルコペニア、フレイル、転倒、低栄養、多剤併用などの老年症候群を約2倍来たしやすい17)。また、高齢者の生活習慣病では食事、内服、注射などのセルフケアができなくなり、介護者がそれらを代わりに行う必要がある。介護者の負担が大きいと、患者自身の心理状態やQOLも低下し、治療を継続することが困難となる。
したがって、高齢期の生活習慣病では合併症を予防するだけでなく、老年症候群を防ぎ、患者だけでなく介護者の負担を軽減することも治療の目的となる(図1)。
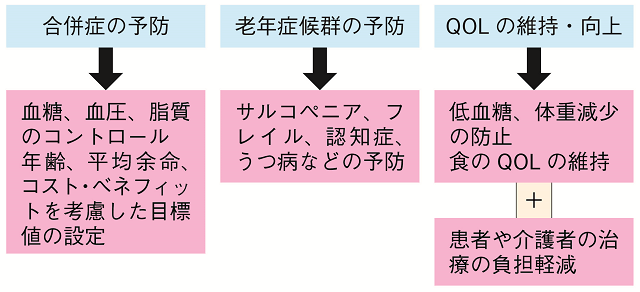
高齢者生活習慣病の管理目標値
高齢者の生活習慣病の管理目標値は年齢だけでなく、認知機能、ADL、有害事象のリスク、併存疾患、平均余命、社会サポートなどに設定することが多い。
多くのガイドラインは年齢によって管理目標値を分けている。高齢者高血圧の降圧薬開始基準と管理目標は病態によって異なる。高齢者の高血圧のガイドラインでは、65~74歳は140/90mmHg以上の血圧レベルを降圧薬開始基準とし、管理目標も140/90mmHg未満とし、75歳以上では150/90mmHgを当初の目標とし、忍容性があれば140/90mmHg未満を降圧目標とするとしている。糖尿病患者や蛋白尿を有する慢性腎臓病(CKD)患者の場合、まず年齢による降圧薬開始基準を目標とし、忍容性があれば130/80mmHg未満を目標とする18)。
高齢者の脂質異常症のガイドラインでは、前期高齢者では一次・二次予防とも基本的に成人と同様のLDLコレステロール管理方針を適応できるとしている19)。75歳以上の後期高齢者の二次予防については、管理目標値の妥当性についてのエビデンスが不十分であるものの、少なくともスタチン投与は有用であると考えられる。一方、後期高齢者の一次予防では、総合的な利益を考慮して、個別に対応する。
高血圧または脂質異常症で高度のフレイルを有する患者では管理目標は個別に判断することになる。
日本糖尿病学会と日本老年医学会の合同委員会では、年齢以外にADL、認知機能によって3つのカテゴリーに分類し、血糖コントロール目標(HbA1c値)を設定している。ADLはADL自立、手段的ADL低下、基本的ADL低下、認知機能は認知機能正常、MCI~軽度認知症、中等度以上の認知症とカテゴリーの段階が進むほど、HbA1cの目標値が高く設定されている。このようにADLや認知機能などの機能障害によって3段階に分けると、機能障害が重症になるにつれて死亡のリスクが高くなることが報告されている20)。
多くの併存疾患や機能低下があるとカテゴリーⅢとなって血糖コントロール目標が高く設定されている。これは多くの併存疾患を伴うと、血糖コントロールの寿命延長効果が乏しくなるからである21)。
このようにADL、認知機能、併存疾患によって死亡のリスク、すなわち平均余命を推定することで、柔軟な管理目標を設定することが、今後、糖尿病だけでなく、他の生活習慣病でも行われることが期待される。
HbA1cの治療目標値は有害事象である低血糖のリスクが危惧される薬剤を使用する場合は目標値が高くなっており、重症低血糖を防ぐために目標下限値を設定している。こうした目標下限値の設定は、IDFや米国糖尿病学会のガイドラインにもみられている。
高齢者生活習慣病の食事療法
高齢者生活習慣病の食事療法は過栄養だけでなく、低栄養に注意することが大切である。特に、75歳以上の後期高齢者では低栄養を来たしやすい。低栄養は体重減少と食事摂取量低下、BMI低値(18.5kg/m2未満)などに注意する。
体重を減らすことは若い人の生活習慣病の食事療法においては重要である。しかし、高齢者で食事療法のみで減量するとサルコペニアが起こる場合がある。減量を行う際には、運動療法を併用することが大切である。
エネルギー制限よりもバランスのとれた食事をすることを中心に栄養指導を行う。バランスのとれた食事とは炭水化物、タンパク質、脂肪の比率が偏らず、ビタミン、ミネラル、食物繊維を十分にとるような食事である。高齢者糖尿病におけるビタミンB群、ビタミンA、食物繊維、緑黄色野菜の摂取不足は認知機能低下の危険因子となる(図2)22)。また、ビタミンB群、ビタミンDなどの摂取不足はサルコペニアまたはフレイルを来たしやすいので注意を要する。
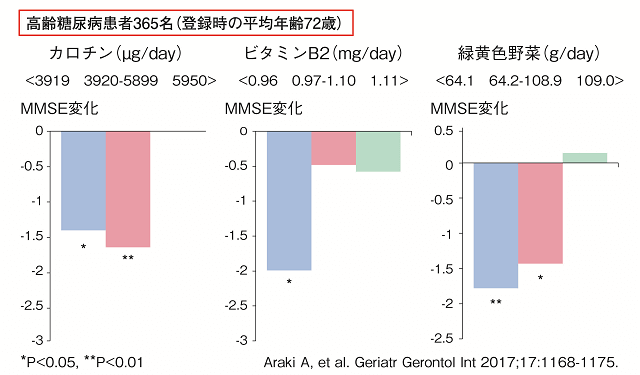
塩分制限(減塩)は糖尿病、高血圧の治療における重要な食事療法の1つである。味覚の加齢変化によって塩分に対する感受性低下を来たし、塩分を過剰摂取している場合もある。また、高血圧の場合、カリウムの摂取不足にも注意する。一方で、低栄養を合併している患者では減塩によって食事摂取が低下し、低栄養を助長する場合もあるので注意を要する。
タンパク質制限は重症の腎機能障害がある場合に行うこと多い。しかしながら、一般の高齢者において筋肉の量と質を保つためには、少なくとも1.0~1.2g/kg体重のタンパク質の摂取を行うことが必要である23)。低栄養または低栄養のリスクがある場合には、1.2~1.5g/kg体重のタンパク質をとることが推奨されている。したがって、高齢者生活習慣病のタンパク質制限は、腎機能低下の速度、血清P値、低栄養やサルコペニアの有無、食事療法のアドヒアランスや意欲を考慮してその適応を決めることが必要である。
栄養指導は患者のADL、認知機能、心理状態、薬剤、併存疾患、社会サポートなどを考慮して、簡易化してアドヒアランスを高めるような工夫をすることが大切である。高齢者は長年の食習慣を変えることが困難であり、複雑な栄養指導はアドヒアランスの低下につながることが多い。1~2個の行うべきポイントを押さえた栄養指導を行うことが望ましい。
高齢者生活習慣病の運動療法
すべての高齢者の生活習慣病において運動療法は最も大切な治療の1つである。第一に、身体活動量を増やすことが大切である。身体活動量を増やすことはADL低下や認知機能低下を防ぎ、血糖、血圧、中性脂肪値を下げ、HDLコレステロール値を上昇させ、インスリン抵抗性を改善し、死亡のリスクを減らすことにつながる。70歳~ 90歳の高齢者糖尿病の追跡調査でも、週4時間以上の身体活動を行っている患者では死亡が少ないという結果が得られている24)。
高齢者が行う運動の種類としては有酸素運動、レジスタンス運動、バランス運動、ストレッチ運動(柔軟性運動)がある。有酸素運動は糖尿病、高血圧、脂質異常症、肥満の治療として大切である。
レジスタンス運動は負荷をかけて筋力トレーニングを行う運動である。高齢者糖尿病やサルコペニア肥満の患者に行うことが勧められる。糖尿病患者における高強度のレジスタンス運動は筋肉量の増加、QOLの向上だけでなく、インスリン抵抗性や血糖コントロールの改善作用を有する25)。
このレジスタンス運動やレジスタンス運動を含む多要素の運動は認知機能低下やフレイル・サルコペニアの悪化の予防に有効である。下肢機能の低下がある高齢糖尿病患者にレジスタンス運動を含む運動を行うと、身体機能のみならず、認知機能も改善する26)。サルコペニアと肥満が合併したサルコペニア肥満の患者に週3回のエラスティックバンドによるレジスタンス運動を12週間行ったRCT研究では、運動介入群は対照群と比べて、除脂肪量と筋肉の質、身体能力が改善し、サルコペニアの頻度が少なくなる27)。
レジスタンス運動は必ずしも高強度でなくても中等度の強度で持続時間を増やせば有効であるといわれている。レジスタンス運動は少なくとも週2回以上行うことが必要である。バランス運動は転倒を防止するために併用することが望ましい。高齢者糖尿病に週2回のレジスタンス運動にバランス運動を併用すると、筋力のみならず、反応時間や姿勢動揺が改善し、転倒リスクが減少すると報告されている28)。
ストレッチ運動は上記の運動の前後で念入りに行うことが運動中の事故や運動後の疼痛の予防のために大切である。
冠動脈疾患、心不全、骨関節疾患、糖尿病増殖性網膜症などの合併がある場合は、事前のメディカルチェックは必須であり、個別の対応を要する。運動を行う場合には脱水、糖尿病患者では低血糖にも注意する。
高齢者生活習慣病の薬物療法
薬物療法は、1.薬物有害事象を防ぐような薬物選択と用量調節、2.服薬アドヒアランスの向上、3.多剤併用(ポリファーマシー)の対策を行うことが大切である。
薬物有害事象では、詳細は各稿に譲るが、脱水や低血糖などの有害事象はシックデイとよばれる発熱や嘔吐、下痢などの消化器症状がある場合に起こりやすいので、シックデイの対策について介護者を含めた教育を行う必要がある。
服薬アドヒアランスの低下は、認知機能障害、手段的ADL低下、うつ、低栄養、多剤併用、家族や社会のサポートが乏しい患者で起こりやすい。薬剤師などと連携しながら、残薬のチェックを行うとともに、服薬ボックスや服薬カレンダーを使用するなどの服薬アドヒアランス改善の工夫を行う。
糖尿病や高血圧などの生活習慣病の患者では多剤併用を来たしやすい。高齢者糖尿病は、合併症や併存疾患が多くなり、多剤併用に至りやすい。オーストラリアの高齢糖尿病患者のデータでは、併存疾患の中央値は5個であり、脂質異常症、高血圧症の併存は60%以上であり、虚血性心疾患は50%以上、胃食道逆流症は46%にみられた29)。
多剤併用の原因として心血管疾患の合併がある。特に糖尿病、虚血性心疾患、脳血管疾患、心不全、心房細動などが同時合併した場合、それぞれのガイドラインを遵守して治療を行えば、多剤併用になりやすくなる。
多剤併用の問題点には、低血糖、転倒など薬物相互作用による有害事象のリスクが高まることや服薬アドヒアランス低下、コストの増大、QOLの低下がある。海外の報告においては多剤併用の対策としては、1.投薬の利益がない薬剤を中止する、2.有害事象がある薬剤を中止する、3.患者の環境を考慮して治療の介入が困難な場合、高額の薬剤の使用を控える、4.認知症などがあり、治療の忍容性が低下した場合、患者のサポートを優先するとしている30)。
本邦では、認知症などで社会サポートが低下した場合、2型糖尿病であれば、頻回のインスリン注射から持効型インスリン1日1回と経口血糖降下薬の併用療法への変換、インスリンから週1回のGLP-1受容体作動薬の注射への変更、可能ならインスリン離脱などを試みることができる。
また、内服薬は服薬タイミングを食直前または食後に統一し、可能な限り1日1 ~ 2回の投薬にすることで単純化を行うことが必要となる。配合剤も降圧剤や経口血糖降下薬で使用可能である。服薬の確認や週1回のGLP-1受容体作動薬の注射のために、訪問看護を利用することもできる。
参考文献
- Pedditizi E, et al. Age Ageing 2016; 45: 14-21.
- Tancredi M, et al. N Engl J Med 2015;373;1720-1732.
- Huang ES, et al. JAMA Intern Med 2014;174: 251-258.
- Krumholz HM, et al. JAMA. 1994;272(17):1335-1340.
- Nagasawa SY, et al. J Am Heart Assoc. 2012;1:e001974.
- Beckett NS, et al. N Engl J Med 2008 ; 358 : 1887-1898.
- SPRINT Research Group, Wright JT Jr, et al. N Engl J Med. 2015; 373 : 2103-2116.
- Hassing LB, et al. Age Ageing 33 : 355-361, 2004.
- Yaffe K, et al. JAMA 2004;292:2237-2242.
- Ninomiya T, et al : Hypertension 2011;58:22-28.
- Morris MC, et al : Arch Neurol 2001;58:1640-1646.
- Wong E, et al.Lancet Diabetes Endocrinol 1: 106-14, 2013
- Balzi D, et al. Age Ageing. 2010;39:92-98.
- Vincent HK, et al. Obes Rev 2010;11:568-579.
- Hirani V, et al. Age Ageing. 2017;46:413-420.
- Melzer D, et al. J Gerontol A Biol Sci Med Sci 2005,60:1319-1323.
- Araki A, Ito H. Geriatr Gerontol Int 2009;9:105-114.
- 「高齢者高血圧診療ガイドライン 2017」 日老医誌 2017;54:1-63.
- 「高齢者脂質異常症診療ガイドライン 2017」日老医誌 2017;54:467-490.
- Cigolle CT,et al. J Gerontol A Biol Sci Med Sci. 2012;67:1313-1320.
- Huang ES, et al. Ann Intern Med 2008;149:11-9.
- Araki A, et al. Geriatr Gerontol Int 2017;17:1168-1175.
- Deutz NE, et al. Clin Nutr 2014;33:929-936.
- Stessman J, J Am Geriatr Soc 2014;62:1329-1334.
- Mavros Y, et al. Diabetes Care 2013;36:2372-2379.
- Espeland MA, et al. J Gerontol A Biol Sci Med Sci 2017;72:861-866.
- Liao CD, et al. Medicine (Baltimore) 2017;96(23):e7115.
- Morrison S, et al. Diabetes Care 2010;33: 748-750.
- Caughey GE, et al: Diabetes Res Clin Pract 2010; 87: 385-393.
- Lipska KJ, et al. JAMA. 2016 Mar 8;315:1034-1045.
筆者

- 荒木 厚(あらき あつし)
- 東京都健康長寿医療センター内科総括部長
- 略歴:
- 1983年:京都大学医学部卒業、同附属病院老年科研修医、1984年:静岡労災病院(現、浜松労災病院)内科研修医、1985年:京都大学医学部大学院入学、1987年:東京都老人医療センター内分泌科医員、1995年:英国ロンドン大学ユニバーシティカレッジ留学、1996年:米国ケースウエスタンリザーブ大学留学、1997年:東京都老人医療センター内分泌科復職、1999年:同内分泌科医長、2006年:同内分泌科部長、2009年:東京都健康長寿医療センター糖尿病・代謝・内分泌内科部長(名称変更)、2012年より現職
- 専門分野:
- 老年医学、糖尿病、病態栄養。医学博士
転載元
機関誌「Aging&Health」アンケート
機関誌「Aging&Health」のよりよい誌面作りのため、ご意見・ご感想・ご要望をお聞かせください。
お手数ではございますが、是非ともご協力いただきますようお願いいたします。
